Page 75 - Revista Islaud 81
P. 75
Evaluación del impacto financiero y el acceso efectivo a tratamientos de alto precio por la Sabrina
introducción de medicamentos biosimilares en el INSSJP‑PAMI entre los años 2018 y 2020 Hnatiw
alrededor de 18 mil unidades dispensadas contra apro‑ intercambiabilidad de los medicamentos biológicos.
ximadamente 17 mil del biosimilar (52:48) La intercambiabilidad hace referencia a la posibilidad
Para bevacizumab, se observó que tanto por con‑ de intercambiar un medicamento por otro que se espera
venio como por licitación una preponderancia del que tenga el mismo efecto clínico. Esto podría significar
Biosimilar en todos los periodos del orden del 70:30 cambiar un producto de referencia por un biosimilar (o
independientemente de la modalidad de adquisi‑ viceversa) o reemplazar un biosimilar por otro. El reem‑
ción. En tanto, en la compra conjunta inicial, la marca plazo puede realizarse mediante: un cambio, que es el
de bevacizumab original adjudicó alrededor de 4 mil proceso por el cual el profesional que extiende la receta
unidades de la concentración por 100 mg y 3.500 de la decide cambiar un medicamento por otro con el mismo
concentración por 400mg, por un total de 137 millones fin terapéutico o una sustitución (automática), que es la
de pesos y en tanto el biosimilar adjudicó unas 9 mil práctica de dispensar un medicamento en lugar de otro
unidades de bevacizumab por 100 mg y 8 mil de 400 medicamento equivalente e intercambiable a nivel far‑
mg, por un total de 329 millones de pesos. macéutico sin consultar con el prescriptor. (EMA, 2019)
Por último, para etanercept la penetración del En algunos países europeos, entre ellos Francia, Ale‑
biosimilar es muy baja alcanzando menos del 10% en mania y España el cambio de un medicamento biológico
2020. Debemos aquí considerar que el original era la innovador o biosimilar por otro debe realizarse bajo la
única alternativa disponible durante un periodo pro‑ responsabilidad del facultativo tratante o siguiendo la
longado de tiempo. política establecida en el centro asistencial, pero siem‑
pre procurando mantener la trazabilidad de las sus‑
El Intercambio o sustitución tituciones realizadas. Esta trazabilidad es altamente
Dentro del mercado de los biológicos, uno de los pun‑ importante, dado que permitirá asociar los efectos ad‑
tos más discutidos probablemente se remita a la sustitu‑ versos, en caso de producirse, a un paciente, a un pro‑
ción o intercambiabilidad de marcas. De hecho, no existe ducto y a un lote determinados. Por ello, la intercambia‑
en la actualidad un consenso a nivel global respecto de la bilidad es posible pero siempre bajo el conocimiento y
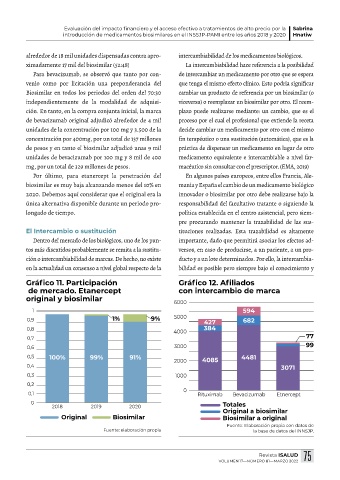
Gráfico 11. Participación Gráfico 12. Afiliados
de mercado. Etanercept con intercambio de marca
original y biosimilar
6000
1 594
0,9 1% 9% 5000 427 682
0,8 4000 384
0,7 77
0,6 3000 99
0,5 100% 99% 91% 2000 4085 4481
0,4 3071
0,3 1000
0,2
0
0,1 Rituximab Bevacizumab Etnercept
0 Totales
2018 2019 2020
Original a biosimilar
Original Biosimilar Biosimilar a original
Fuente: Elaboración propia con datos de
Fuente: elaboración propia la base de datos del INNSJP.
Revista ISALUD 75
VOLUMEN 17—NÚMERO 81—MARZO 2022